Was macht oncgnostics genau?
Die Diagnose Krebs hat trotz vieler Fortschritte in der Medizin ihren Schrecken nicht verloren. Im Gegenteil: Erkrankten doch 2012 weltweit über 14 Millionen Menschen an Krebs, über 8 Millionen starben an einer Krebserkrankung – Tendenz noch immer steigend.
Die meisten Krebserkrankungen sind inzwischen sehr gut behandelbar – allerdings nur, wenn sie rechtzeitig erkannt werden. Für viele Krebserkrankungen fehlen derzeit zuverlässige Methoden, die einen frühzeitigen Nachweis ermöglichen. Dieses Problems nehmen wir uns an: oncgnostics entwickelt spezielle Tests für eine zuverlässige Krebsdiagnostik!
UNSER ERSTES AKTIONSFELD – GEBÄRMUTTERHALSKREBS
Dank der Einführung von regelmäßigen Vorsorgeuntersuchungen über den sogenannten Pap-Abstrich ist Gebärmutterhalskrebs in den Industriestaaten in den letzten vierzig Jahren sehr viel seltener geworden. Den Pap-Abstrich können in Deutschland Frauen ab 20 Jahren jährlich in Anspruch nehmen, über 16 Mio. dieser Tests werden auch tatsächlich jedes Jahr durchgeführt. Dennoch wurden allein in Deutschland im Jahr 2012 noch immer 4.640 neue Fälle diagnostiziert, 1.617 Frauen starben (www.krebsdaten.de). Dies liegt zum Einen daran, dass etliche Frauen (etwa 35 %) die Vorsorgeuntersuchungen nicht wahrnehmen, zum Anderen daran, dass immer noch Erkrankungen beim Pap-Abstrich übersehen werden.
Früh erkannt, sind Gebärmutterhalskrebs und dessen Vorstufen zu nahezu 100 % heilbar – eine bessere Diagnostik kann also Leben retten!
GEBÄRMUTTERHALSKREBS IST AUS MEHREREN GRÜNDEN UNGEWÖHNLICH:
-
Der Krebs wird durch eine Infektion mit sogenannten humanen Papillomviren (HPV) verursacht. Die werden überwiegend durch Geschlechtsverkehr übertragen. Allerdings verschwinden die meisten Infektionen wieder – nur selten führen sie zu Krebs.
-
Von der Infektion bis zur Ausbildung von Krebs kann es sehr lange dauern, meist über 10 Jahre.
-
In der Krebsentstehung treten Gewebeanomalien (Krebsvorstufen) auf, die als Krebsvorstufen bezeichnet werden. Pathologen unterscheiden bei diesen Gewebeanomalien die Stufen CIN1, 2 oder 3, die sich alle im Mikroskop untereinander sowie von Krebsgewebe unterscheiden. Alle diese Vorstufen gelten als auffällige Befunde, aber nur ein Bruchteil dieser Vorstufen entwickelt sich tatsächlich zur bösartigen Krebserkrankung. Selbst CIN3, die am weitesten fortgeschrittene Gewebeveränderung, entwickelt sich nicht immer zu einer Krebserkrankung weiter.
-
Es sind vor allem junge Frauen betroffen: Gebärmutterhalskrebs wird am häufigsten im Alter von 40 bis 50 Jahren festgestellt. Gewebeanomalien werden aber schon bei 20- bis 30-jährigen Frauen diagnostiziert – und das oft fälschlich.
WELCHES PROBLEM LÖST ONCGNOSTICS?
Das Hauptproblem der derzeitigen Vorsorgemethoden besteht darin, dass sie nicht gut zwischen einer harmlosen Abnormalität, die von allein wieder verschwindet, und einer ernstzunehmenden Gewebeanomalie, die sich zu Krebs entwickeln kann, unterscheiden können. Eine vorschnelle und teils eben unnötige Therapie, bei der Teile des Muttermundes und Gebärmutterhalses operativ entfernt werden, ist oft die Folge.
Auffällige bzw. abklärungsbedürftige Ergebnisse werden bei etwa 1,5-2 % der untersuchten Frauen beim Pap-Abstrich erhalten. Bei den betroffenen Frauen treten dann viele Fragen auf: „Kann sich bei mir Krebs entwickeln? Wann weiß ich das? Wann muss ich wieder zur Untersuchung kommen und was ergibt sich dann? Welche Risiken hat eine mögliche Operation für mich und wie ist das, wenn ich später Kinder bekommen möchte?“
VIDEO
Dr. med. Jörg Herrmann, Chefarzt der Klinik für Gynäkologie und Geburtshilfe in Weimar, zur momentanen Vorsorge und die Einsatzmöglichkeiten von GynTect®.
UNSERE LÖSUNG: GYNTECT® WEIST KREBSSPEZIFISCHE MARKER NACH
Unser erster Test namens GynTect® ist für genau DIE Frauen entwickelt, die nach einem auffälligen Pap-Abstrich oder nach dem Nachweis einer Infektion mit HPV unsicher sind: „Bekomme ich oder habe ich Krebs?“ Bei nur wenigen Frauen besteht wirklich Handlungsbedarf, denn nur wenige haben bei einem auffälligen Pap-Abstrich oder einem positiven HPV-Test eine bösartige Veränderung. GynTect® zeigt zuverlässig, welche dieser Frauen Krebs entwickeln könnten und welche nicht.
Ein negativer GynTect®-Test gibt Entwarnung: Es sollte keine Krebsvorstufe vorliegen. Die Patientin sollte im Rahmen der üblichen Routine – meist nach etwa einem Jahr – untersuchen lassen, ob auch die HPV-Infektion wieder verschwunden ist bzw. die Zellen im Pap-Abstrich wieder normal aussehen. Liegt wieder ein auffälliger Pap-Abstrich bzw. eine HPV-Infektion vor, sollte auch GynTect® wiederholt werden.
Ein positiver GynTect®-Test gibt Klarheit: Die Patientin wird zum Spezialisten geschickt. Dieser sucht in einer Spezialuntersuchung mit einer Lupeneinrichtung, dem Kolposkop, genau die Stelle am Muttermund, an der die Veränderung, die zu einem positiven GynTect®-Testergebnis geführt hat, auftritt. Je früher diese Stelle entdeckt wird, desto kleiner kann der operative Eingriff – die sogenannte Konisation, bei der diese Stelle entfernt wird – ausfallen.
VIDEO
Welchen Vorteil bietet mir denn nun GynTect®? Petra und Susanne erklären, welchen Nutzen GynTect® direkt für die einzelne Frau hat.
WARUM GYNTECT® SO WICHTIG IST
Diagnosen auf vermeintliche Krebsvorstufen werden ganz oft bei jungen Frauen zwischen 20 und 35 Jahren gestellt. Gerade bei jungen Frauen heilen solche vermeintlichen Vorstufen häufig ohne Behandlung aus und könnten kontrolliert beobachtet werden. Dennoch erhalten viele junge Frauen eine Operation, eine sogenannte Konisation, die sie nicht brauchen.
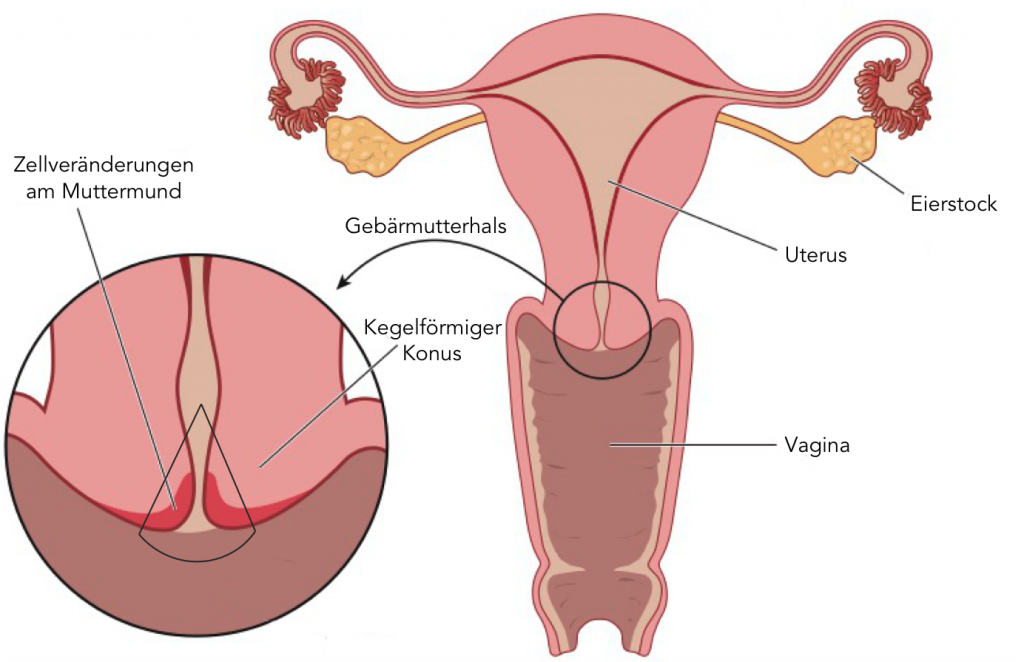
Abbildung 1: Bei der Konisation wird aus dem Gebärmutterhals ein kegelförmiges Gewebestück rund um den Muttermund entfernt. Das Gewebestück wird dann unter dem Mikroskop untersucht, um festzustellen, ob das auffällige Gewebe vollständig entfernt wurde. Mit GynTect® können unnötige Eingriffe dieser Art verhindert werden.
Bei Frauen mit Konisation treten bei Schwangerschaften in der Folge bis zu 10 mal häufiger Fehl- oder Frühgeburten auf. Dieses erhöhte Risiko können all diejenigen vermeiden, die bei einem negativen GynTect®-Testergebnis gar nicht erst operiert werden. Bei positivem GynTect®-Ergebnis kann die Operation hingegen frühzeitig durchgeführt und somit der Eingriff so klein wie möglich gehalten werden. Da GynTect® sehr zuverlässige Ergebnisse liefert, profitieren davon alle.
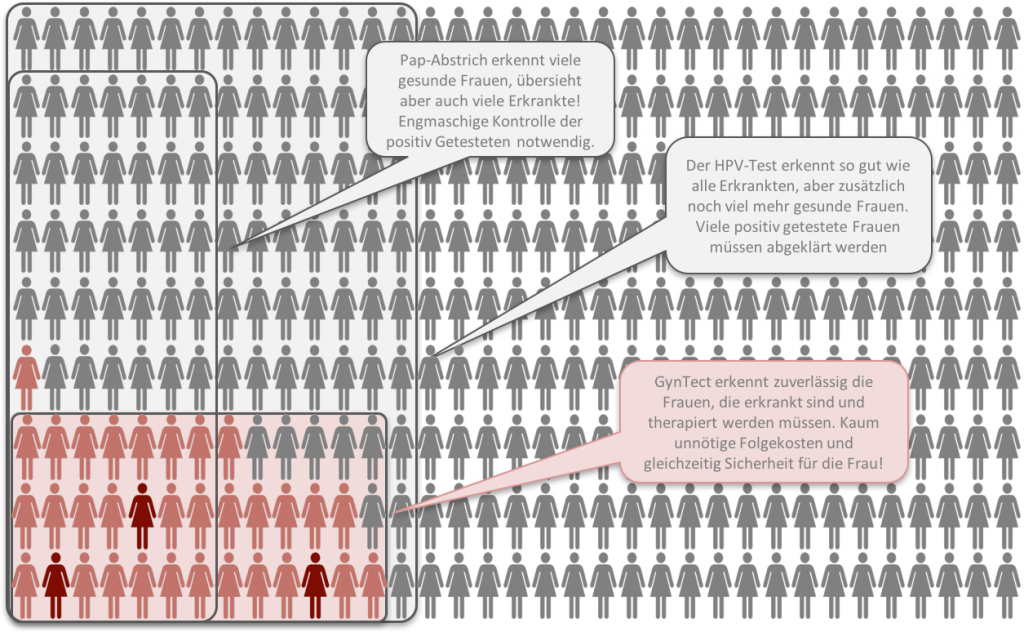
Abbildung 2: Ein zuverlässiger Test bzw. eine gute Testkombination erkennt unter den vielen Frauen, die eine Erkrankung haben können (gesamte Population der Frauen > 20 Jahre), diejenigen, die tatsächlich diese Erkrankung gerade entwickeln oder haben (Frauen mit HPV-Infektion UND Veränderung im Gewebe, die zu Krebs führt (rosa) oder sich bereits zu Krebs entwickelt hat (dunkelrote)).
WORAUF BERUHT GYNTECT®?
Unsere Tests weisen sogenannte epigenetische Marker nach, die speziell nur in der Erbinformation von Krebszellen auftreten. Und die meisten dieser Veränderungen treten für jede Krebsart an unterschiedlichen Stellen in der Erbinformation auf. Daher war es möglich, solche epigenetischen Marker für Gebärmutterhalskrebs zu identifizieren und aus diesen GynTect® zu entwickeln.
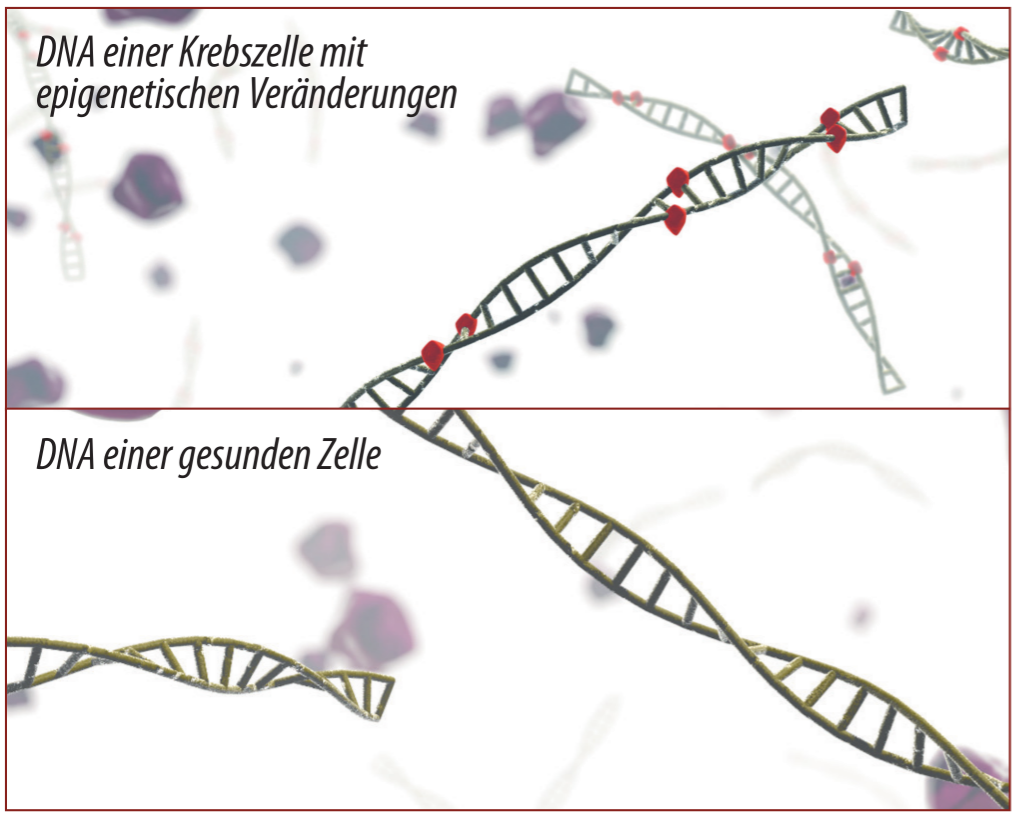
Abbildung 3: Epigenetische Veränderungen, die wir nachweisen, finden direkt an der Erbinformation, der DNA, statt. Diese Veränderungen sind krebsspezifisch, so dass für jede Krebserkrankung eigene Marker definiert werden können.
Unsere epigenetischen Krebsmarker haben viele Vorteile, die wir für Betroffene nutzbar machen wollen:
- Die Marker sind sehr robust, sie verändern sich nicht während Entnahme, Transport und Lagerung.
-
Die Marker sind im molekulardiagnostischen Labor einfach nachweisbar.
-
Die Marker liefern zuverlässige Ergebnisse in kurzer Zeit.
-
Das bedeutet: Sicherheit für Betroffene.
Wir identifizieren für unterschiedliche Krebserkrankungen solche veränderten Regionen in der Erbinformation, testen diese hinsichtlich ihrer Eignung für die jeweilige Anwendung in der Diagnostik: Das bedeutet, wir testen die identifizierten Marker an einer Vielzahl von klinischen Proben. Die sehr gute Zusammenarbeit mit dem Universitätsklinikum Jena sowie anderen Kooperationspartnern erlaubt es uns, identifizierte Marker anhand einer großen Sammlung an sehr gut charakterisiertem klinischen Material auf ihre Zuverlässigkeit zu testen. Darauf beruhend entwickeln wir diagnostische Tests – für eine schnellere, zuverlässigere und effektivere Krebsdiagnostik.
Was ist seit dem letzten Funding passiert?
Mit unserem ersten Crowdfunding im Sommer 2016 wollten wir zum Einen weitere Schritte für die Vermarktung von GynTect® finanzieren. Zum Anderen wollten wir das Problem der unzureichenden Krebsvorsorge in die Crowdfunding-Community tragen und damit Frauen in die Lage versetzen, das Thema mit ihrem Frauenarzt auf Augenhöhe zu besprechen und mit GynTect® eine neue Lösung ins Spiel zu bringen.
Vor unserem ersten Funding letztes Jahr konnten wir noch keine nennenswerten Umsätze erzielen. Seitdem ist es uns gelungen, eine Vereinbarung für eine exklusive Lizenz für Herstellung und Vertrieb von GynTect® in China zu schließen. Neben Meilensteinzahlungen in siebenstelliger Höhe werden wir auch an Umsätzen unseres chinesischen Partners GeneoDx, eine Tochterfirma des staatlichen Sinopharm-Konzerns, beteiligt sein. Derzeit arbeiten wir am Abschluss von Vertriebspartnerschaften in weiteren Märkten speziell in Europa, aber auch außerhalb Europas. Für den kanadischen Markt haben wir bereits ein Vertriebsabkommen geschlossen. Dort ist GynTect® gerade im Registrierungsprozess.
Die Vermarktung von GynTect® wird auch durch eine zweite CE IVD Zulassung erleichtert: Seit einem Jahr liegt eine Version vor, bei der das Abstrichmaterial, das für die mikroskopische Untersuchung sowie für viele unterschiedliche HPV-Tests genommen wird, auch für GynTect® eingesetzt werden kann. In manchen Ländern, darunter auch die USA, erleichtert dies enorm den Einsatz von GynTect®.
Weiterhin ist es uns gelungen, ein Kooperationsprojekt einzuwerben, das uns bei der Automatisierung von GynTect® sowie bei unseren Pipeline-Projekten einen wichtigen finanziellen Beitrag verschafft. Ein weiteres Entwicklungsprojekt steht kurz vor der Genehmigung.
Woher stammt die Idee?
Die Idee für GynTect® kommt aus dem gynäkologischen Forschungslabor am Universitätsklinikum Jena, das von Prof. Dr. Matthias Dürst geleitet wird. Er forscht bereits seit über 30 Jahren am Zusammenhang zwischen der Infektion mit HPV und der Entstehung von Gebärmutterhalskrebs. In seiner Doktorarbeit hat er den besonders aggressiven Virus des Typs HPV16 beschrieben, den er aus Krebsgewebe isoliert hat. Sein Doktorvater Professor Harald zur Hausen hat, aufgrund dieser bahnbrechenden Forschungen, 2008 den Nobelpreis für Medizin erhalten. Gebärmutterhalskrebs ist seit diesen Forschungen auch die erste Krebsart, gegen die eine Impfung existiert. Allerdings wirkt die Impfung nicht bei allen krebsauslösenden Viren.
Dr. Alfred Hansel, Geschäftsführer der oncgnostics GmbH, hat im Labor von Prof. Dr. Matthias Dürst nach den oben genannten epigenetischen Unterschieden zwischen normalen Zellen und Krebszellen gesucht, die heute die Grundlage für den fertigen Test GynTect® darstellen. Dr. Martina Schmitz, heute Co-Geschäftsführerin und Laborleiterin bei oncgnostics, stieg 2010 in das Projekt ein. Gleiches gilt für Kerstin Brox, die sich seither um die Finanzen bei oncgnostics kümmert. Alle Gründer von oncgnostics treibt die Vision an, eine sehr schnelle und genaue Diagnostik zu entwickeln. Die GynTect® zugrundeliegende Technik hat sich als sehr robust erwiesen. Deshalb soll sie mit dem Investment der Crowd auch in den weiteren Entwicklungsprojekten von oncgnostics, Diagnostik bei Eierstockkrebs sowie bei Kopf-Hals-Tumoren eingesetzt werden.
Was macht oncgnostics einzigartig?
GynTect®, das erste Produkt von oncgnostics, basiert auf Veränderungen, die in der DNA von Tumorgewebe direkt vorliegen, also echten Krebsmarkern.
-
Verglichen mit anderen Tests hat GynTect® eine bessere Erkennung von zu therapierenden Krebsvorstufen und Krebszellen (= hohe Sensitivität).
-
Mit GynTect® werden deutlich weniger gesunde Patientinnen als vermeintlich krank erkannt (= hohe Spezifität) wie mit den momentan verwendeten Tests.
-
Die GynTect®-Marker könnten einen prognostischen Wert haben: Das heißt, sie sind in der Lage anzuzeigen, in welchen Fällen sich aus einer Gewebeveränderung eine Krebserkrankung entwickeln wird und, in welchen Fällen eine solche Veränderung wieder ausheilt, ohne dass Krebs entsteht. Diese Eigenschaft hat kein am Markt verfügbarer Test, ein Alleinstellungsmerkmal von GynTect®. Eine Studie, die diese Charakteristik von GynTect® belegen soll, ist in Vorbereitung.
Die von oncgnostics bei GynTect® eingesetzte Technologie-Plattform der epigenetischen Marker lässt sich auch auf weitere Diagnostikfelder anwenden. In den von uns derzeit bearbeiteten Feldern, nämlich Eierstockkrebs und Kopf-Hals-Tumore, stehen heute noch keine Früherkennungs-Tests zur Verfügung, und es werden Therapien durchgeführt, die nicht bei allen Patienten Aussicht auf Erfolg haben (wie z. B. Chemotherapien bei platin-resistentem Eierstock-Krebs und Kopf-Hals-Tumor-Patienten). Die von oncgnostics entdeckten Marker-Panel für diese Anwendungen sollen für den hohen medizinischen Bedarf in diesen Bereichen entwickelt werden.
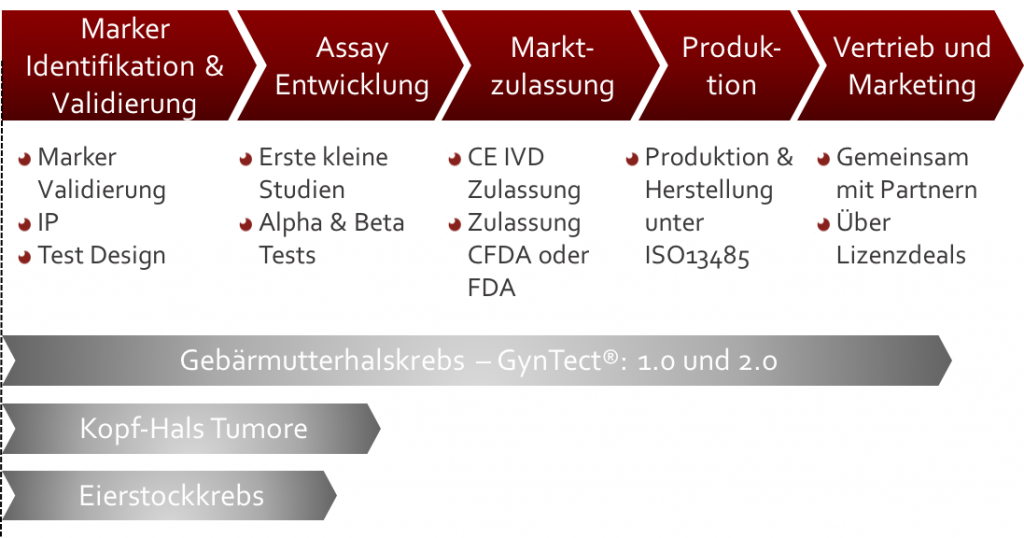
Abbildung 4: Stand der oncgnostics-Projekte. Während GynTect® zur Marktreife entwickelt ist, arbeiten wir in unseren beiden Pipeline-Projekten „Kopf-Hals-Tumoren“ und „Eierstockkrebs“ derzeit an der Validierung der dafür identifizierten Marker sowie den ersten Schritten zur Assayentwicklung.
Warum eine Anschlussfinanzierung? Warum wieder Seedmatch?
Das erste Seedmatch-Crowdfunding plus die Spiegelung durch die bm-t haben uns sowohl bei der Vermarktung von GynTect® als auch beim Bekanntmachen unseres Testkonzeptes sehr geholfen. Dafür sind wir allen Investoren sehr dankbar! Jetzt wollen wir den nächsten Schritt gehen. Wir haben bereits beim ersten Funding verdeutlicht, dass wir weiteres Kapital einwerben wollen, um den eingeschlagenen Weg erfolgreich abzuschließen. Allerdings hatten wir eine größere Investitionsrunde angekündigt, die zu einer deutlichen Verwässerung der Crowd geführt hätte. Wie oben geschildert haben wir inzwischen zum einen Lizenzzahlungen erhalten und zum anderen Projektmittel eingeworben, was unseren Bedarf an externem Kapital für die nächsten Jahre substanziell verringert. Daher ist es uns möglich, mit einer weiteren Investmentrunde, an der bestehende Investoren sowie die Crowd teilnehmen, unsere Ziele ebenfalls zu erreichen. Da die Unternehmensbewertung in diesem Fall nur moderat höher als in der ersten Finanzierungsrunde liegt, ist auch die Verwässerung geringer. Und Sie erhalten nochmals die Möglichkeit, an unserem zukünftigen wirtschaftlichen Erfolg teilzuhaben!
Wie generiert oncgnostics Umsätze?
Der Nachweis der speziellen Marker macht den Markenkern von GynTect® aus: Ihre Anwendung in der Krebsdiagnostik ist patentgeschützt, so dass nur wir diese Marker für unsere Produkte nutzen können. Will eine andere Firma unsere Marker nutzen, muss sie also bei uns eine Lizenz kaufen. Der Patentschutz gilt für die wesentlichen Märkte (US, EU, JP, CA) für einen Test wie GynTect®, für weitere Märkte haben wir zwei Patentschriften zu den GynTect®-Markern eingereicht.
Fest steht: Wir wollen GynTect® weltweit anbieten. GynTect® ist fertig entwickelt und hat zudem die CE IVD-Zulassung für sämtliche EU-Länder sowie einige weitere Länder, so dass Testkits nach lokaler Registrierung verkauft werden können und der Test für Patientinnen angewendet werden kann. Für die Vermarktung kommen verschiedene Möglichkeiten in Frage:
-
Vertrieb von GynTect®-Testkits über Händler, die in dem Marktsegment bereits Produkte vertreiben.
-
Vergabe von lokalen oder auch weiter reichenden exklusiven Lizenzen für GynTect®-Marker an Local oder Global Player im Bereich Krebsdiagnostik.
-
Strategische Partnerschaft mit einem Global Player in einem der Bereiche Pharma/Gesundheit/ Diagnostik.
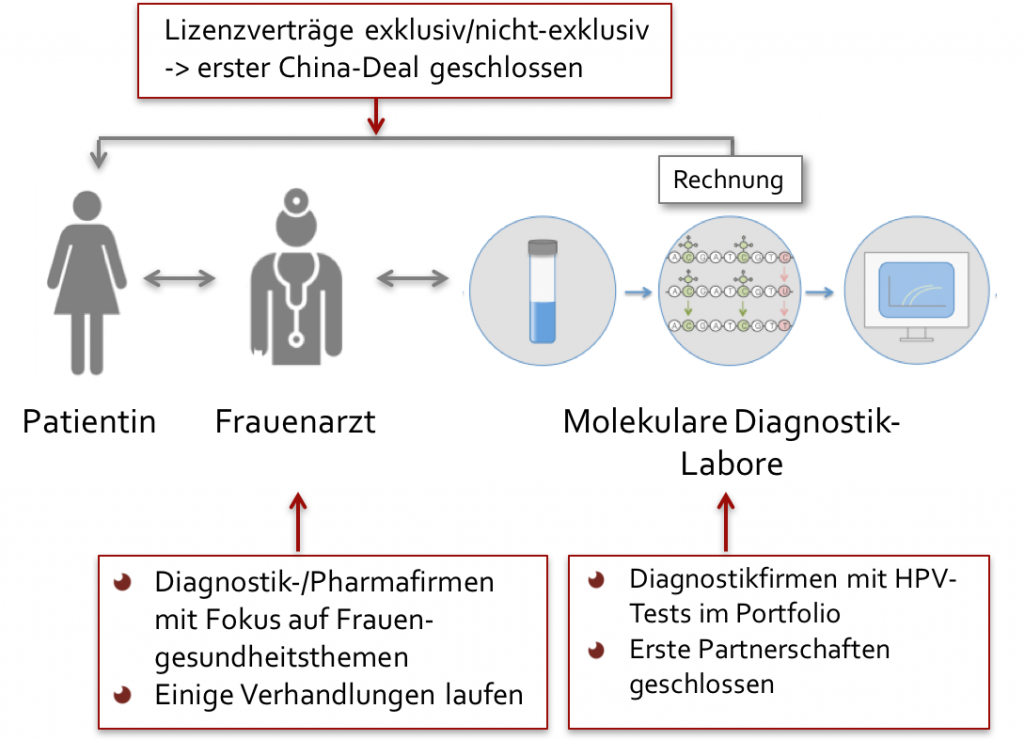
Abbildung 5: Vermarktung von GynTect über mehrere Kanäle: Firmen aus dem Bereich Frauengesundheit überzeugen Frauenärzte von unserem Konzept; diese empfehlen ihren Patientinnen den Test; Diagnostiklabore, die den Test durchführen, machen ihn ebenfalls bei Ärzten bekannt.
Für den chinesischen Markt haben wir kürzlich eine exklusive Lizenzvereinbarung geschlossen: unser Partner GeneoDX, eine Tochterfirma des staatlichen SINOPHARM-Konzerns, betreibt derzeit die Zulassung für den chinesischen Markt. Für den Technologietransfer erhalten wir in Meilensteinen eine siebenstellige Summe, danach sind wir am Vermarktungserlös beteiligt. Desweiteren wurden GynTect®-Kits für Forschungszwecke von GeneoDx bestellt. Für einige Europäische Märkte sowie Kanada haben wir bereits Vermarktungsvereinbarungen geschlossen bzw. sind im Gespräch. Hier erwarten wir für 2018 erste substanzielle Umsätze in sechsstelliger Höhe.
Alle diese Vermarktungsaktivitäten sind Vorbereitung für das Ziel, die Auslizenzierung von GynTect® an Global Player im Bereich Molekulare Diagnostik zu realisieren. In diesem Markt werden Milliarden umgesetzt: Die USA ist im Bereich molekulare Diagnostik global das Land mit dem höchsten Marktanteil (ca. 45 %), gefolgt von der EU (25 %) und Japan (10 %). In diesem Bereich wurden im Jahr 2015 3,21 Mrd. Dollar allein im US-Markt umgesetzt, ein jährliches Wachstum von 12,5 % wird prognostiziert. Der Teilbereich der onkologischen Diagnostik wächst sogar noch stärker, ca. 18 % jährliches Wachstum wird für die nächsten Jahre angenommen. (Frost & Sullivan, The US Molecular Diagnostics Market, Forecast to 2021, Report K0AD-52, Nov 2016). In allen genannten Regionen gilt für GynTect® Patentschutz!
WIE SIEHT DER MARKT FÜR GYNTECT® AUS?
DER BESTEHENDE MARKT FÜR GYNTECT®
GynTect® ist ein Abklärungstest für Frauen, die einen auffälligen Befund aus dem Pap-Abstrich oder/und ein positives HPV-Testergebnis erhalten haben und wissen wollen: „Habe ich Krebs? Muss ich mich jetzt wirklich operieren lassen?“
Jährlich werden allein in Deutschland über 16 Millionen Pap-Abstrichuntersuchungen gemacht, und dabei gibt es über 200.000 abklärungsbedürftige Ergebnisse (Befund Pap III, Pap IIID; Mühlhauser, 2008, http://www.arznei-telegramm.de/html/2008_03/0803029_01.html). Bei ihnen kann GynTect® Klarheit schaffen. Es gibt jährlich bis zu 90.000 Operationen (https://www.thieme-connect.de/products/ejournals/html/10.1055/s-0034-1368588), von denen sehr viele nicht durchgeführt werden müssten, wenn vorher eine Abklärung durch GynTect® erfolgen würde. Eine zuverlässige Diagnostik, wie GynTect® sie erlaubt, könnte einen großen Teil dieser Operationen verhindern.
DER MARKT FÜR GYNTECT® WÄCHST SUBSTANZIELL!
Bei uns in Deutschland soll sich ab 2018 für Frauen ab 35 Jahren die Früherkennung von Gebärmutterhalskrebs stark ändern: Sie erhalten dann sowohl einen Pap-Test als auch einen HPV-Test. Sind beide negativ, erfolgt die nächste Vorsorgeuntersuchung erst wieder in drei Jahren. Ist einer der Tests hingegen positiv, muss abgeklärt werden. Je nach Schweregrad der Vorbefunde ist GynTect® hierfür geeignet.
In anderen europäischen Märkten (z. B. Niederlande) sowie in den USA wird der HPV-Test bereits als Eingangstest neben dem Pap-Test in der Vorsorge eingesetzt. Hier besteht somit ein deutlich größerer Bedarf für eine bessere Abklärung. Sobald in der EU und in den USA nur noch HPV-Tests als primärer Test in der Krebsvorsorge verwendet werden, ergäbe sich die folgende Marktsituation:
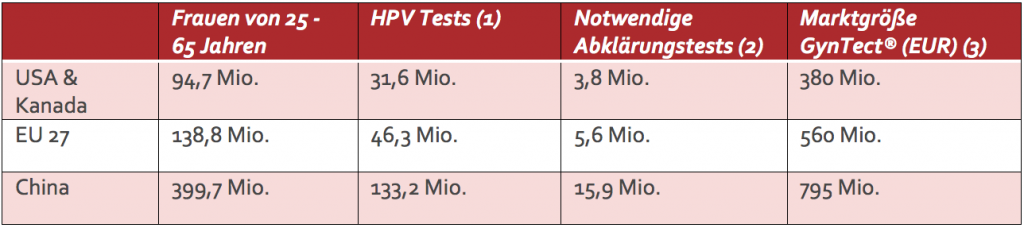
Abbildung 6: Zielgruppen für die Gebärmutterhalskrebs-Vorsorge und daraus resultierendes Marktpotenzial für GynTect®. Annahmen hierbei: (1) bei negativem Ergebnis wird der HPV-Test alle drei Jahre wiederholt; (2) etwa 15 % der HPV-Tests fallen positiv aus; (3) Kostenannahme für GynTect® 100 EUR in USA&Kanada, EU, 50 EUR in China. „Frauen von 25 – 65 Jahren“: Bevölkerungsstatistiken 2015 für EU und Nordamerika sowie China.
Für den Vertrieb im riesigen und sehr attraktiven US-Markt wird eine weitere Zulassung durch die FDA (US Food and Drug Administration) notwendig. Diesen Prozess wollen wir mit einem starken strategischen Partner angehen, der im US-Markt im Bereich Diagnostik und Frauengesundheit unterwegs ist. Für den chinesischen Markt haben wir mit GeneoDx, einem Tochterunternehmen des großen staatlichen SINOPHARM-Konzerns, hierfür bereits genau den richtigen exklusiven Lizenzpartner. Mit einem Vermarktungsstart rechnen wir hier, nach Zulassung von GynTect® durch die CFDA (China Food and Drug Administration), die unser chinesischer Partner derzeit betreibt, in 2019. An den Umsätzen sind wir beteiligt.
WO EIN MARKT IST, SIND WETTBEWERBER!
Wir sind auf dem Markt Früherkennung von Gebärmutterhalskrebs nicht allein: Zur Abklärung von auffälligen Pap-Abstrichen und positiven HPV-Ergebnissen wurden auch von anderen Firmen Tests entwickelt. Diese zeigen allerdings eine schlechtere klinische Performance als GynTect®, sind also fehleranfälliger. Entscheidend ist, dass ein solcher Test bei allen Erkrankten positiv sein muss, während er bei möglichst wenigen „Gesunden“ falsch positiv sein sollte, um Unsicherheit sowie unnötige Kosten durch Übertherapie zu vermeiden.
-
Roche Diagnostics: CINtec plus ist ein Färbetest auf einem Zellabstrich. Der Test ist bei zu vielen „Gesunden“ positiv. Es wird kein echter Krebsmarker nachgewiesen.
-
Qiagen hat zwei Marker der niederländischen Firma Self-Screen einlizensiert, bietet damit den Test QIAsure auf Basis der gleichen Technologie wie GynTect®, aber mit anderen Markerregionen an. Auch hier zeigt GynTect® eine deutlich bessere klinische Performance.
Wer steht hinter oncgnostics?

Abbildung 7: Unser Team (v. l. n. r.): Anne Hengst, Kristin Eichelkraut, Dana Schmidt, Anna-Bawany Hums, Dr. Martina Schmitz, Dr. Alfred Hansel, Dr. Juliane Hippe, Kristina Wunsch, Carolin Dippmann, Kerstin Brox, und Dr. Peter Haug
Gegründet wurde oncgnostics Anfang 2012 von den beiden Geschäftsführern Dr. Martina Schmitz und Dr. Alfred Hansel gemeinsam mit Prof. Dr. Matthias Dürst und Kerstin Brox. Inzwischen sind wir ein starkes Team von 10 Leuten, das viel Enthusiasmus, aber auch viel Erfahrung in den Gebieten Forschung, Entwicklung, Produktion, all das in einer ISO13485-zertifizierten Umgebung mit dem notwendigen Qualitätsmanagement sowie Business Development vereint.
MANAGEMENT
Dr. Alfred Hansel ist als Geschäftsführer unter anderem speziell für Geschäftsentwicklung und strategisches Partnering zuständig. Er hat langjährige Erfahrungen im Bereich der Projektführung durch Arbeiten an inländischen und ausländischen universitären Einrichtungen. Operative Erfahrungen in der Industrie hat Dr. Alfred Hansel in den Unternehmensbereichen Produktentwicklung, Sales und Marketing in der Firma Jena Bioscience GmbH erworben und bei oncgnostics weiter ausgebaut. Als Molekularbiologe hat er im Labor von Prof. Dürst die Grundlagen für GynTect, Identifikation und wissenschaftliche Validierung der Marker, gelegt.
Dr. Martina Schmitz ist als Geschäftsführerin unter anderem für die Leitung des Labors und damit auch für die Entwicklung und Zulassung der diagnostischen Tests der oncgnostics GmbH verantwortlich. Aufgrund ihrer langjährigen Tätigkeit im Labor “Gynäkologische Molekularbiologie” unter der Leitung von Prof. Dürst hat sie sich nicht nur mit den Grundlagen der Entstehung von Gebärmutterhalskrebs intensiv auseinandergesetzt (Promotion), sondern auch bereits Erfahrungen mit der Entwicklung eines Nachweis-Tests für HPV (Diplomarbeit) gesammelt.
Kerstin Brox leitet den Bereich Finanzen der oncgnostics GmbH seit Firmengründung. Sie hat unter anderem 12 Jahre im privaten Kreditgeschäft einer Bank sowie über vier Jahre im Einkauf bei einer lokalen Marketingagentur gearbeitet.
Dr. Peter Haug hat sieben Jahre Beratungserfahrung in der Chemiebranche und fünf Jahre Industrieerfahrung aus der Pharmabranche. Dort war er verantwortlich für Verträge, Kooperationen sowie Übernahmen von Standorten der großen Pharmakonzerne mit insgesamt über 1.500 Mitarbeitern und einem Verkaufsvolumen von insgesamt über 250 Mio. €. Seit 2011 ist er als Founding Angel spezialisiert auf junge Unternehmen und unterstützt als solcher auch die oncgnostics GmbH im Bereich Business Development und Exit-Anbahnung.
Prof. Dr. Matthias Dürst leitet seit 1997 den Funktionsbereich „Gynäkologische Molekularbiologie“ an der Universitätsfrauenklinik Jena und ist ausgewiesener Experte im Bereich der humanen Papillomaviren, Krebsentstehung und HPV-Diagnostik. Prof. Dürst hat wesentliche Beiträge zu den Forschungsarbeiten geleistet, die 2008 zur Vergabe des Nobelpreises für Medizin an Herrn Prof. Dr. Harald zur Hausen führten. Seine langjährigen Erfahrungen im Bereich der virusinduzierten Karzinogenese und seine Kontakte zu Wirtschaft und Wissenschaft stellt er als Gründer und Kooperationspartner für die oncgnostics GmbH zur Verfügung.
LABOR- UND ENTWICKLUNGSTEAM

Unser starkes Forschungs- und Entwicklungsteam hat es zusammen mit dem Management innerhalb kürzester Zeit geschafft, einen Laborbetrieb neu aufzubauen und ein funktionierendes Qualitätsmanagement-System nach der Medizinproduktenorm ISO13485 zu etablieren. Dieses QM-System ist für die Bereiche Forschung, Entwicklung und Produktion von einer autorisierten externen Firma, der DQS Medizinprodukte, geprüft und zertifiziert. Mit GynTect® haben wir den ersten molekulardiagnostischen Test bis zur Marktreife entwickelt, wir produzieren ihn auch in einem hierfür zugelassenen Labor.
Eine solche Leistung schafft man nur mit einem starken und hoch motivierten Team!
Dana Schmidt, Biotechnologin, bringt ihre inzwischen 10-jährige Entwicklungserfahrung und ihre Sorgfalt nicht nur in die Testentwicklung, sondern als QM-Beauftragte auch in die Organisation des Qualitätsmanagements von oncgnostics ein.
Anne Hengst, ebenfalls Biotechnologin, unterstützt Dana Schmidt in beiden Bereichen, übernimmt zudem wesentliche Aufgaben in der Entwicklung sowie in der Produktion.
Labororganisation und praktische Arbeiten, vor allem für Studien, liegen in den Händen unserer sehr erfahrenen technischen Mitarbeiterin Kristina Wunsch.
Nachdem Kristin Eichelkraut in unserem Labor bereits ihre Masterarbeit absolviert hat, verstärkt sie unser Team in Forschung und Entwicklung sowie in der Produktion, ist zudem für das Kundenmanagement zuständig.
Seit dem Abschluss der praktischen Arbeiten für ihre Doktorarbeit kümmert sich Dr. Juliane Hippe neben Mitarbeit in der Entwicklung speziell um Forschung in unseren Pipeline-Projekten, bei denen es um Eierstockkrebs sowie um Kopf-Hals-Tumoren geht.
Bawany Hums verstärkt den Bereich F&E seit Abschluss ihrer Masterarbeit, in welcher sie sich intensiv mit epigenetischen Markern bei Eierstockkrebs auseinandergesetzt hat. Neben Routinearbeiten übernimmt sie Forschungsarbeiten speziell in unseren Pipeline-Projekt Kopf-Hals-Tumore.
Des Weiteren ist Carolin Dippmann seit Juni 2017 als Doktorandin bei uns tätig. Ihre Doktorarbeit beschäftigt sich mit der Biologie der GynTect® Marker.
Wir beschäftigen im Labor immer Studenten für Abschlussarbeiten zu verschiedenen Aspekten aus den Bereichen Forschung und Entwicklung. So halten wir zum Einen engen Kontakt zur akademischen Forschung und haben zum Anderen die Möglichkeit, frühzeitig interessante Kandidaten für die Mitarbeit in der Firma zu identifizieren.
Partner und Netzwerk
UNSER BEIRAT
Ein hochkarätig und ausgewogen besetzter Beirat berät uns regelmäßig in unseren Aktivitäten.
Prof. Dr. Ingo B. Runnebaum, MBA und Direktor der Klinik und Poliklinik für Frauenheilkunde und Fortpflanzungsmedizin, Universitätsklinikum Jena, ist Gynäkologe, Krebsforscher, Reproduktionsmediziner sowie Universitätsprofessor der Friedrich-Schiller-Universität Jena mit den wissenschaftlichen Schwerpunkten Gynäkologische Onkologie, gynäkologische Chirurgie und gynäkologische Molekularbiologie. Er ist anerkannter Experte auf dem Gebiet des Ovarial-, Zervix- und Mammakarzinoms und mit seiner Klinik schon immer wichtiger Kooperationspartner der oncgnostics GmbH.
Prof. Dr. Magnus von Knebel Doeberitz, Direktor Angewandte Tumorbiologie, Universitätsklinikum Heidelberg, war Mitgründer der Firma mtm laboratories, die 2011 sehr erfolgreich an Roche Diagnostics verkauft wurde. Er hat daher neben seinem medizinisch-wissenschaftlichen Hintergrund auch wertvolle Erfahrungen hinsichtlich Ausgründung und Marktpositionierung im Bereich Gebärmutterhalskrebsdiagnostik und ist anerkannter Experte auf diesem Gebiet.
Dr. Christoph Petry, Inhaber und Geschäftsführer der Petry Life Sciences Consulting GmbH, hat langjährige Erfahrungen im Bereich der Diagnostik. Als promovierter Chemiker leitete er unter anderem die Diagnostikabteilung der Bayer HealthCare AG und der Siemens Healthcare Diagnostics, ehe er selbst die Sividon Diagnostics gegründet hat. Zuletzt war er dort als CEO für die unterschiedlichsten Unternehmensbereiche zuständig. Er hat die Firma von der Gründung zum erfolgreichen Exit durch Verkauf an die Myriad Genetics geführt.
KOOPERATIONSPARTNER
Durch unsere langjährige berufliche Tätigkeit in Forschung und Industrie haben wir sehr wertvolle Kooperationen mit vielen für den Geschäftserfolg von oncgnostics wichtigen Personen, Forschungseinrichtungen und Unternehmen etabliert.
WISSENSCHAFTLICHE UND KLINISCHE KOOPERATIONSPARTNER
Unsere Entwicklungen wären nicht möglich ohne unsere klinischen Kooperationspartner des Universitätsklinikums Jena. Sie bringen klinisches Know-how und Anwenderwissen, Forschungskapazität für Kooperationsprojekte sowie Probenmaterial für die Entwicklung und Validierung unserer Tests in die Firma. Die prospektive, multizentrische Beobachtungsstudie wird ebenfalls in Kooperation und unter der Leitung von Herrn Prof. Matthias Dürst (Leiter des Fachbereiches Gynäkologische Molekularbiologie der Frauenklinik Jena) und des Zentrums für klinische Studien durchgeführt. Für die Entwicklung von GynTect® sowie für unsere Pipeline-Projekte im Bereich Eierstockkrebs arbeiten wir eng mit der Universitäts-Frauenklinik Jena zusammen. Für unsere weiteren Pipeline-Projekte im Bereich Kopf-Hals-Tumore kooperieren wir eng mit der HNO-Klinik des Jenaer Universitätsklinikums.
oncgnostics ist Mitglied beim infectoGnostics Forschungscampus. Das Netzwerk verfolgt das Ziel, Lösungen für die schnelle, zuverlässige und kostengünstige Vor-Ort Analyse von Infektionen und Infektionsbedingten Erkrankungen zu erforschen und mit industriellen Partnern in marktreife Lösungen zu überführen. Im Rahmen dieses Netzwerkes nehmen wir am BMBF-geförderten Projekt ASSURER teil, das eine (Teil-)Automatisierung des GynTect®-Assays sowie die Etablierung der Marker im Bereich Eierstockkrebs-Früherkennung zum Ziel hat.
Wir arbeiten weiterhin mit wissenschaftlichen und klinischen Partnern an unterschiedlichen Kliniken in Deutschland sowie mit niedergelassenen Ärzten zusammen, die unser Testkonzept für GynTect® mit uns in Studien weiter etablieren wollen.
KOOPERATIONSPARTNER AUS DEM BEREICH DIAGNOSTIK
Tests wie GynTect® werden in unabhängigen Laboren durchgeführt, die für diesen Zweck die von uns produzierten Kits kaufen. Wir kooperieren mit einigen solchen Laboren im In- und Ausland bereits seit der Testentwicklung, um Rückmeldung zu erhalten, ob es Schwierigkeiten bei der Testbearbeitung gibt. Diese Kooperationspartner kommen dann auch schnell für die Durchführung unserer Tests in Frage, sobald diese zugelassen sind.
UNSERE INVESTOREN

Der High-Tech Gründerfonds investiert Risikokapital in junge, chancenreiche Technologie-Unternehmen, die vielversprechende Forschungsergebnisse unternehmerisch umsetzen.

Die Stiftung für Technologie, Innovation und Forschung Thüringen (STIFT) fördert im Rahmen des Thüringer Netzwerkes für Innovative Gründungen (ThürInG) innovative und technologieorientierte Gründungen in Thüringen. Zudem unterstützt STIFT ausgewählte High-Tech Gründungen im Bereich der Frühphasenfinanzierung als Side-Investor.

Die bm|t beteiligungsmanagement thüringen GmbH mit Sitz in Erfurt ist eine Tochter der Thüringer Aufbaubank und erste Adresse für Beteiligungen in Thüringen. Die bm|t führt aktuell acht Fonds mit einem investierten Gesamtvolumen von rund € 320 Millionen, die sich an innovativen Unternehmen nahezu aller Branchen und in allen Phasen der Unternehmensentwicklung – sowohl in der Gründungs- als auch in der Wachstumsphase oder in Unternehmensnachfolgesituationen beteiligen.

Die Sparkasse Jena-Saale-Holzland ist seit mehr als 185 Jahren ein starker und verlässlicher Partner in der Region Jena und Saale-Holzland. Durch das große Filialnetz sind die Berater für Ihre Kunden in unmittelbarer Nähe und treffen wichtige Entscheidungen schnell und direkt vor Ort. Vom Girokonto über Immobilienvermittlung und Baufinanzierung bis hin zur Firmen- und Gewerbekundenbetreuung bietet die Sparkasse alles aus einer Hand. Als öffentlich-rechtliches Institut ist sie dem Gemeinwohl, der Wirtschaftsförderung in der Region und den Menschen, die hier leben, verpflichtet.

Anastasia Borghardt ist Geschäftsführende Gesellschafterin der ITAI GmbH Aschaffenburg. Diese investiert vorwiegend in mittelständische Unternehmen die perspektivisch in nachhaltigen und wachsenden Märkten bereits erfolgreich sind, bzw. werden können. Zukunftsorientierte, innovative und technisch ausgeprägte Produkte sind dabei entscheidende Kriterien.
Wo steht oncgnostics und wo geht es hin?
Seit unserer Gründung Anfang 2012 haben wir bei oncgnostics innerhalb kurzer Zeit sehr viel erreicht. Wir haben
-
für GynTect® die CE IVD Zulassung für den Europäischen Markt erhalten,
-
in ersten Kooperationen bzw Lizenzvereinbarungen den Markt für GynTect® addressiert und erste Umsätze generiert und
-
bereits seit Gründung den eigenen F&E-Laborbetrieb sowie die von uns aufgebauten Produktionslabore unter zertifiziertem Qualitätsmanagement (ISO13485) etabliert,
Seit unserer ersten Crowdfunding-Runde im Sommer 2016 haben wir uns kontinuierlich weiterentwickelt:
-
Wir haben eine weitere Zulassung für unseren Test GynTect® erhalten, die den Einsatz in vielen Märkten erleichtert. Der Test passt nun in Konzepte, bei denen aus bereits vom Screeningtest (HPV- oder Pap-Test) vorhandenem Material der Patientin eine Abklärung gemacht werden soll.
-
Wir haben den Test an unseren Partner GeneoDX, Shanghai, China, auslizenziert und damit einen der größten Märkte für GynTect® erschlossen! Dies bedeutet für uns Umsätze in Millionenhöhe in Form von Meilensteinzahlungen bereits für die Lizenzvereinbarung, den Technologietransfer und die Marktzulassung durch unseren chinesischen Partner, sowie eine Umsatzbeteiligung. Die erste Meilensteinzahlung ist bereits in Q2 2017 geflossen, die zweite erwarten wir spätestens für Q1 2018.
-
Wir haben eine Vermarktungsvereinbarung für den kanadischen Markt sowie Vorvereinbarungen für einige EU-Märkte geschlossen. Weitere Verhandlungen sind auf dem Weg. Hier erwarten wir erste Umsätze in 2018.
-
Wir haben Studien abgeschlossen und die Ergebnisse in wissenschaftlichen Zeitschriften publiziert (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5655856/) sowie auf internationalen Fachkonferenzen präsentiert. Publikationen zu weiteren Studien sind in Arbeit und werden demnächst erscheinen.
Unsere erste Crowdfunding-Runde hat bereits neben der substanziellen finanziellen Unterstützung auch zur breiteren Diskussion unseres GynTect-Konzepts beigetragen. Jedoch ist einem Großteil der Frauenärzte und Patientinnen das Konzept GynTect® noch immer unbekannt. Dieses wollen wir mit der zweiten Kampagne ändern und die Verbreitung intensivieren.
In einigen europäischen Ländern stehen wir kurz vor Abschluss von Vertriebsvereinbarungen. Mit dem Geld aus dieser zweiten Finanzierungsrunde mit der Crowd wollen wir diesen Prozess fortführen und GynTect®, unser erstes Produkt, erfolgreich in weitere spannende Märkte bringen, speziell in die USA. Dazu ist es notwendig, weitere Studien durchzuführen, die Ergebnisse und das GynTect-Konzept auf internationalen Messen und Konferenzen zu präsentieren und mit möglichen strategischen Partnern in Verhandlungen zu treten. Im deutschen Markt wollen wir die Notwendigkeit unseres GynTect-Konzepts durch die Einbindung der Botschafterin der Krebsvorsorge, Myriam von M, besser bekannt machen. Als eine von Gebärmutterhalskrebs selbst Betroffene hat sie sich mit ihrer Fuck Cancer gGmbH das Ziel gesetzt, die Bedeutung der Krebsvorsorge und die Problematik einer eindeutigen Abklärung viel mehr in die Öffentlichkeit zu tragen. Durch ihre Aktivitäten in sozialen Medien – allein auf ihrer Facebook-Seite hat sie über 190.000 direkte Follower – sowie ihre Auftritte in Funk, Fernsehen und Printmedien ist sie ein idealer Multiplikator für unser diagnostisches Konzept hier in Deutschland, dem am schwierigsten zu gewinnenden Markt.
Die Learnings aus der erfolgreichen GynTect-Entwicklung fließen in unsere Pipeline-Projekte im Bereich Eierstockkrebs sowie Kopf-Hals-Tumoren ein. Für diese Felder mit sehr hohem medizinischen Bedarf wollen wir mit unseren klinischen Kooperationspartnern diagnostische Tests entwickeln. Hierfür konnten wir zusätzlich auch Projektmittel einwerben. Die Abbildung verdeutlicht den derzeitigen Stand bei diesen Projekten, sowie die noch notwendigen Schritte bis zu einer möglichen Markteinführung.
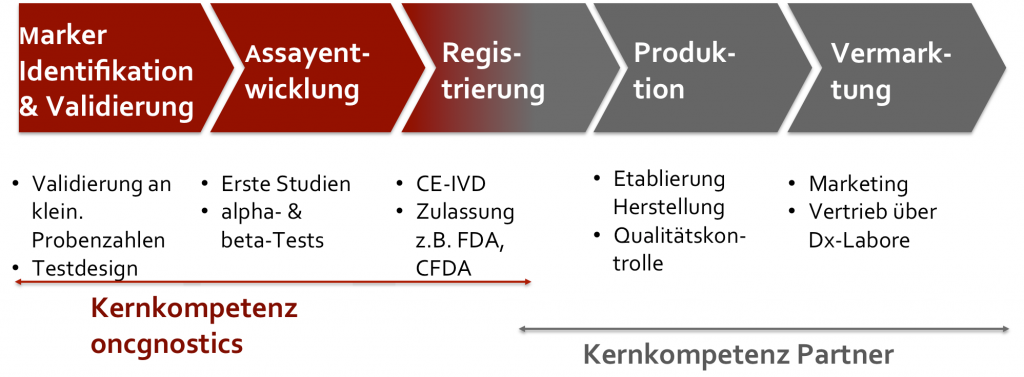
Abbildung 8: Unsere Kernkompetenz liegt in den Bereichen Markeridentifikation und Validierung, gemeinsam mit klinischen Partnern, sowie der Assayentwicklung. Mit GynTect® haben wir sehr viel Erfahrung auf regulatorischer Ebene gesammelt, da wir hierfür die Zulassung für Europa selbst durchgeführt haben. Außerdem sind wir in der Lage, den Test selbst zu produzieren. Dennoch sind dies Aufgaben, die wir prinzipiell gemeinsam mit entsprechenden strategischen Partnern angehen würden.
Mittelverwendung und Fundingstufen
Unser bisheriger Investorenkreis unterstützt unseren eingeschlagenen Weg voll und ganz. Von der Tatsache, dass wir keine große Finanzierungsrunde mit entsprechenden Verwässerungseffekten schließen, profitieren letztlich alle. Durch die Einwerbung von Projektmitteln können wir es schaffen, mit der Summe aus dem Crowdfunding sehr weit zu kommen. Die bm|t hat auch dieses Mal wiederum ihr starkes Interesse bekundet, mit der Crowd zu investieren. Damit können wir die im folgenden aufgeführten Ziele je Fundingstufe noch schneller erreichen.
ERREICHEN DER FUNDINGSCHWELLE 100.000 €
Wir haben weitere Studien zur Performance und Positionierung von GynTect® weitgehend abgeschlossen. Diese werden wir nun publizieren und die Ergebnisse bei Veranstaltungen, z. B. beim Deutschen Krebskongress im Februar 2018 in Berlin präsentieren. Bei solchen Foren bietet sich die Möglichkeit, mit Klinikern das Konzept weitergehend zu diskutieren und somit die Akzeptanz von GynTect® bei medizinischen Experten sowie bei Diagnostikfirmen zu erhöhen – und damit die Absatzchancen! Zudem möchten wir GynTect® auf der molekulardiagnostischen Plattform von Roche etablieren, da diese in immer mehr medizinischen Laboren zum Standard zählt und damit von immer mehr Kunden angefragt wird.
ERREICHEN DES ERSTEN ZWISCHENZIELS 250.000 €
Wir wollen Vermarktungskooperationen mit Partnern in europäischen Märkten abschließen, die unseren Umsatz mit GynTect®-Tests stark voranbringen werden. In der Slowakei und Tschechien verhandeln wir derzeit Vertragsdetails mit Partnern mit einer starken Marktposition im Bereich Diagnostik dieser beiden Länder. Gleiches gilt für den portugiesischen Markt, wo wir ebenfalls einen erfahrenen Distributor sowie eines der größten Labore des Landes von GynTect® überzeugen konnten. Technisch möchten wir GynTect® für ein weiteres Abstrich-Entnahmemedium etablieren, das in ausgewählten europäischen Ländern einen hohen Marktanteil hat. Mit den dann drei Zulassungen (GynTect 1.0, GynTect 2.0 und GynTect 3.0) können wir nahezu alle bei Gynäkologen verwendeten Abstrichmedien verwenden, was die Akzeptanz und Vertriebsmöglichkeiten weiter steigert.
ERREICHEN DES ZWEITEN ZWISCHENZIELS 500.000 €
Wir wollen eine Erhebung zur psychologischen Belastung von Patientinnen mit unklarem Vorsorgeergebnis durchführen, um auf dieser Basis wichtige Interessengruppen noch gezielter überzeugen zu können.
Des Weiteren führen wir eine retrospektive outcome-basierte Studie mit hohem Evidenzlevel durch. Eine derartige Studie macht oncgnostics bei strategischen Partnern im Diagnostikbereich noch interessanter. Sie hilft zudem, auf dieser Basis die Erstattungsfähigkeit von GynTect® bei den Krankenkassen zu erreichen.
ERREICHEN DES FUNDINGLIMITS 750.000 €
Wir intensivieren das Marketing für GynTect®, um strategische Partner für die gemeinsame Vermarktung oder aber interessierte Unternehmen für eine Auslizenzierung zu überzeugen. Speziell zielen wir auf den Nordamerikanischen Markt, da hier die großen Player im Bereich molekulare Diagnostik sowie Frauengesundheit sitzen. Zudem stellt der amerikanische Markt mit seinem Gesundheitssystem und dem bereits etablierten Gebärmutterhalskrebsscreening den für uns attraktivsten Markt dar. Er ist aber auch mit am schwierigsten zu entern! Am Ende könnte auch eine Beteiligung eines Strategen bei oncgnostics oder gar die Übernahme stehen – der Exitfall für alle Investoren!
Nutzen Sie Ihre Chance und investieren Sie in…
-
das marktreife Produkt GynTect® – und helfen Sie so, Frauen ihre Ängste durch unklare Befunde aus der derzeitigen Vorsorge auf Gebärmutterhalskrebs zu nehmen!
-
einen Markt mit hohem, stetig wachsendem Bedarf an innovativer Diagnostik. Hier hat allein GynTect® weltweit ein Milliardenpotenzial.
-
ein hochmotiviertes junges Team, das alle notwendigen Fachkompetenzen für die Entwicklung weiterer molekularbiologischer Tests vereint – und das sich inzwischen auch die entsprechende Marketingkompetenz erarbeitet hat, wie die die erfolgreiche Auslizenzierung an die Sinopharm-Gruppe zeigt.
-
eine Firma mit starken wissenschaftlichen, klinischen und wirtschaftlichen Kooperationspartnern. Dadurch kann oncgnostics sehr schnell und valide neue innovative Diagnostiktests entwickeln.
-
das enorme Potenzial unseres diagnostischen Testkonzepts, das wir auch bei anderen Krebsarten anwenden werden – und damit in eine hohe Renditechance für die Crowd. GynTect® ist erst der Anfang unserer innovativen Diagnostik.
oncgnostics in den Medien
PRESSE
IQ Innovationspreisträger Mitteldeutschland, Cluster Life Science
Pressemitteilung 26.07.2017
GynTect bald in China verfügbar
Pressemitteilung 05.04.2017
MEDICA 2016: oncgnostics präsentiert erweiterten Gebärmutterhalskrebstest GynTect
Innovations Intelligenz, 10.11.2016
Vertriebspartner für oncgnostics
Transkript, 24.06.2016
„Wir wollen die Akzeptanz von GynTect erhöhen“
Going Public online, 21.06.2016
oncgnostics: Test zugelassen
Transkript, 18.09.2015
bm|t, HTGF u.a. investieren siebenstelligen Betrag für oncgnostics
VC-Magazin, 29.01.2015
oncgnostics auf der MEDICA 2015
Homepage MEDICA 06.11.2015
MEDIEN
Sonderpreis für junge Unternehmen im Rahmen des Thüringer Innovationspreises 2014
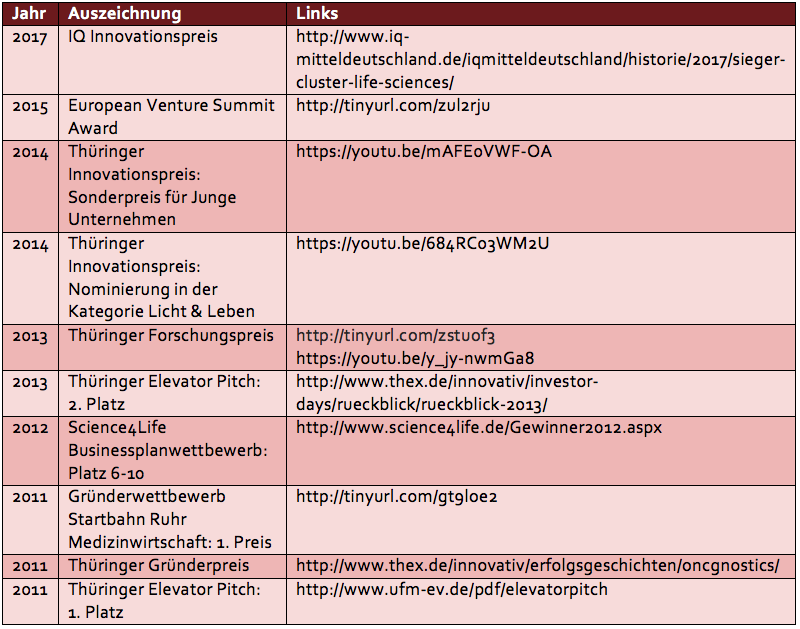
Auszeichnungen

Goodies und Rabatte für Investoren
AB 500 € INVESTMENT

Die Kaffeerösterei Markt 11 in Jena produziert in traditioneller Trommelröstung aus Kaffeebohnen unterschiedlichster Herkunft hervorragende Kaffees für sehr hohe Ansprüche für das eigene Kaffeehaus, den lokalen Markt sowie via Internet für anspruchsvolle Kunden auch weiter entfernt. Da die Ansprüche an unsere Diagnostik genauso hoch sind, das perfekte anregende Dankeschön für ein Investment ab 500€: Ein Paket (500g) Peru Yanesha, ein fair gehandelter, biologisch-dynamischer Hochlandkaffee, den wir bei uns in der Firma bereits seit einiger Zeit genießen.
AB 1.000 € INVESTMENT

für Invests ab 1000 € gibt es zu dem Jenaer Kaffee gleich noch die passende Tasse speziell für unterwegs dazu! Kahla Porzellan steht für die Entwicklung von innovativem Design und Kombination ungewöhnlicher Materialien mit neuen funktionellen Eigenschaften. Unser letztjähriges Goodie, der Cup-It To Go Becher, hat in den letzten Monaten gleich mehrere Preise für Design und Nachhaltigkeit erhalten. Deshalb gibt es dieses Dankeschön auch bei dieser Crowdinvesting-Runde, allerdings in neuem Design! Sie investieren also nicht nur bei uns, Sie haben auch noch die Chance, durch Einsatz unseres Goodies, sich an der Verringerung des täglichen Müllbergs an Pappbechern zu beteiligen, die nach dem „Kaffee unterwegs“ im Abfall landen.
ACHTUNG: neue Kampagne, neues Becherdesign!
Übertragbarer Gutschein für GynTect® Testdurchführung (zusätzlich zu 1 Kaffeebecher & Kaffee)
Sie kennen jemanden, die für einen GynTect®-Test in Frage kommt? Oder wollen selber getestet werden? Beim Frauenarzt wird ein Abstrich genommen und an das oncgnostics-Labor zur Untersuchung gesandt. Das Ergebnis wird an den Frauenarzt übermittelt und er bespricht es dann mit der Patientin. Der Gutschein ist zeitlich nicht limitiert und ist übertragbar.
Die ersten 50 Investoren die 1000 € oder mehr investieren, erhalten zwei CAFÉ SOMMELIER To Go Becher statt nur einem. Dazu ebenfalls den GynTect®-Test für sich oder eine Person der Wahl!
AB 5.000 € INVESTMENT
(zusätzlich zu 1 Kaffeebecher und einem übertragbaren Gutschein für eine GynTect® Testdurchführung)
Ein Abend mit Vertretern des Gründer-Teams am Firmenstandort Jena: Erhalten Sie einen Einblick direkt in unsere Arbeit, danach einen Eindruck von unserer Stadt nebst einem Dinner in gehobener Jenaer Gastronomie!
BEI 10.000 € INVESTMENT
(zusätzlich zu 1 Kaffeebecher und einem übertragbaren Gutschein für eine GynTect® Testdurchführung)
Ein Abend mit Vertretern des Gründer-Teams am Firmenstandort Jena: Neben Einblick, Eindruck und Dinner gibt es eine Übernachtung in herausragender Hotellerie.
Seed Investment: Ihr Renditepotenzial als Investor
Mit einem „Seed Investment“ in oncgnostics haben Sie die Chance auf mehrfaches Renditepotenzial:
Interaktiver Rendite-Rechner
Unternehmens- und Kontaktdaten
oncgnostics GmbH
Winzerlaer Str. 2
07745 Jena
Telefon: 03641 508456
E-Mail: seedmatch@oncgnostics.com
Website: www.oncgnostics.com
Facebook:https://www.facebook.com/oncgnostics/
Handelsregisternummer: HRB 507678
Amtsgericht: Jena
Gründungsdatum: Februar 2012
Geschäftsführer: Dr. Alfred Hansel, Dr. Martina Schmitz
VIB
Vermögensanlagen-Informationsblatt: VIB oncgnostics GmbH
Über oncgnostics 2
oncgnostics - innovative Tests für schnelle, zuverlässige und effektive Krebsdiagnostik










